Projects
1. ゲノム編集を使ったゲノムヒト化
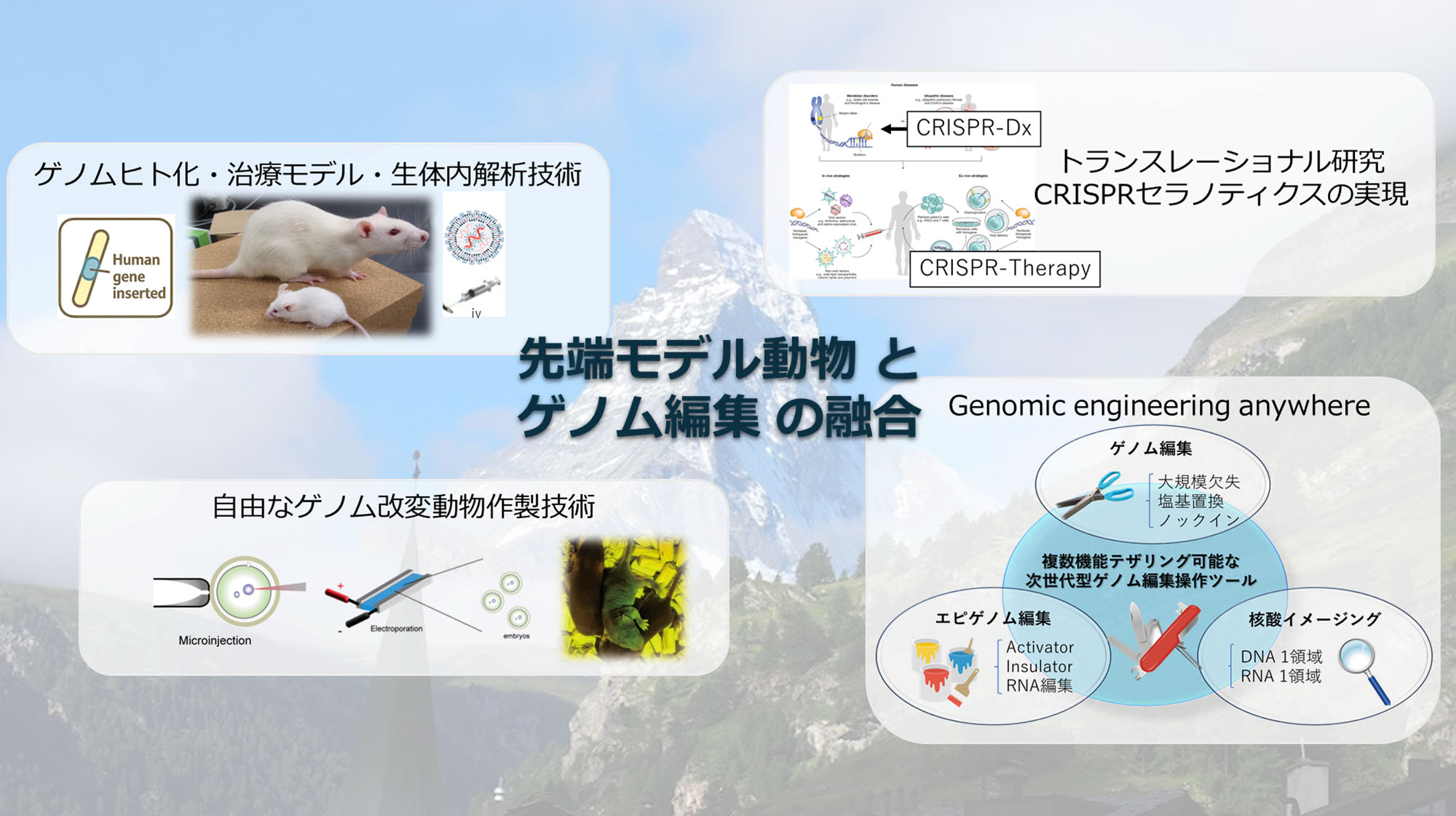
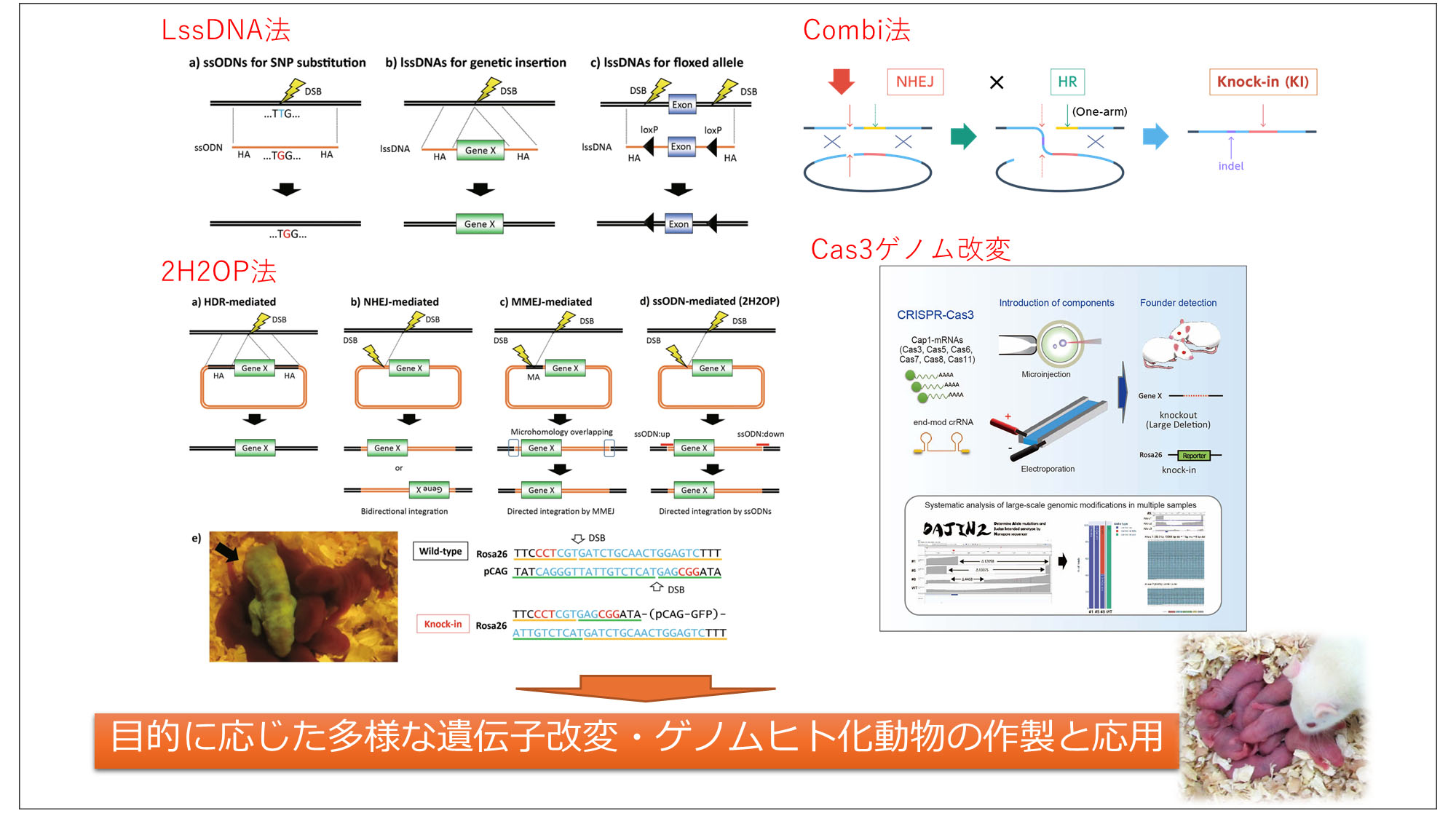
ヒト疾患の発症機構を理解し、新しい治療法の開発につなげるためには、ヒト遺伝子機能を生体内で解析できるモデルが重要です。我々は、ゲノム編集技術を用いたゲノムヒト化研究を進めています。これまでに、ヒト遺伝子領域を効率的に導入するための「2H2OP法」や「Combi法」などのゲノムヒト化技術を開発してきました。今後は、より大規模なヒト遺伝子領域の置換を可能にする新しいゲノムヒト化技術の確立を目指します。また、腸管免疫関連遺伝子をヒト化した腸内細菌叢模倣モデルの構築や、核酸医薬やゲノム編集治療の評価に利用できるヒト化モデルの開発にも取り組み、次世代医療研究の基盤となる実験動物モデルの創出を目指します。
Representative publications
・Yoshimi K, et al. ssODN-mediated knock-in with CRISPR-Cas for large genomic regions in zygotes. Nat Commun. 2016 Jan 20;7:10431.
・Yoshimi K, et al. Combi-CRISPR: combination of NHEJ and HDR provides efficient and precise plasmid-based knock-ins in mice and rats. Hum Genet. 2021 Feb;140(2):277-287.
2. 次世代ゲノム操作技術の開発
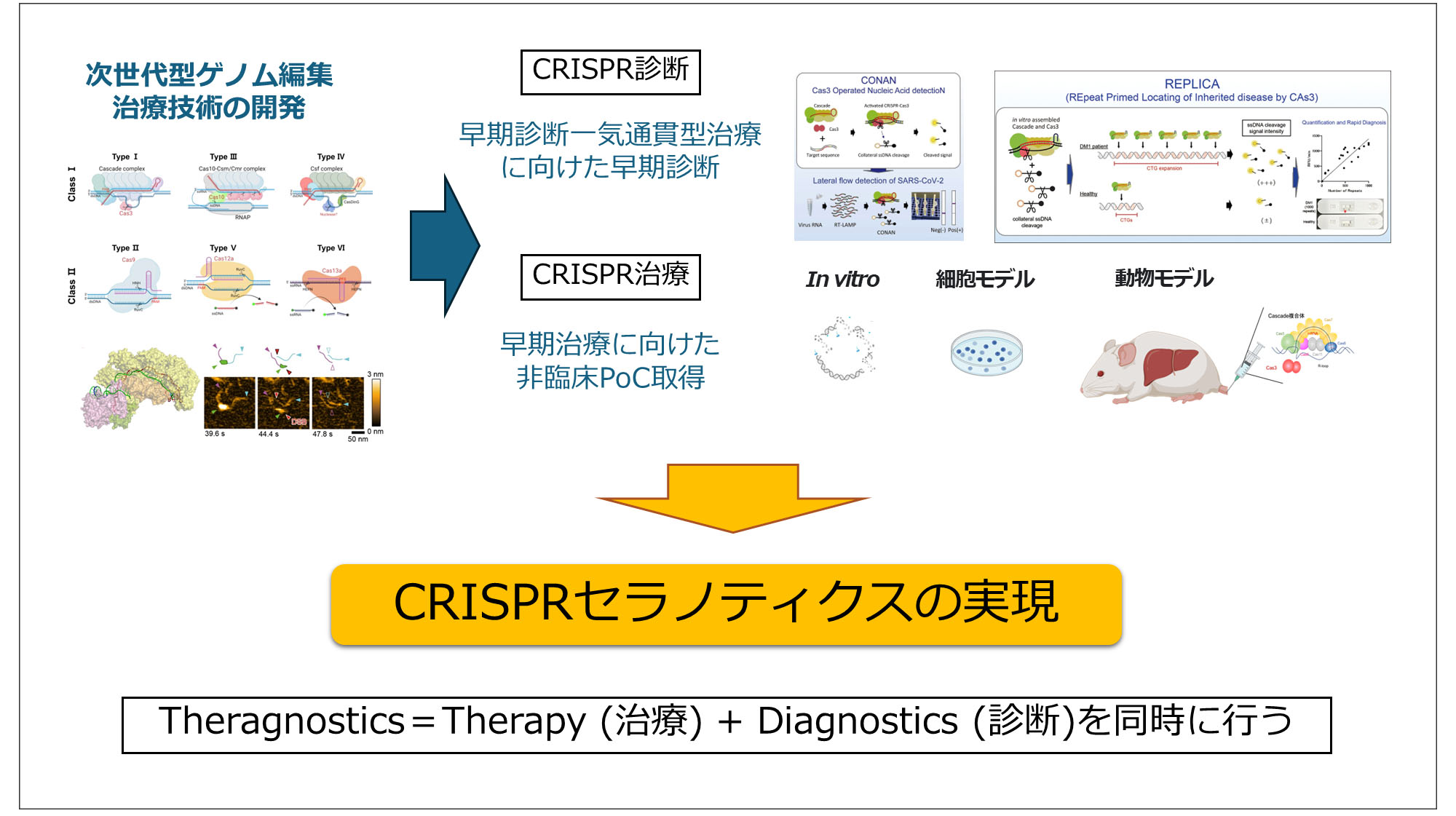
ゲノム編集技術は生命科学研究の基盤技術となりつつあり、医療や産業分野への応用も急速に広がっています。本研究室では、これまでに「CRISPR-Cas3」を用いた新しいゲノム編集技術の開発に取り組み、基礎研究から医療・産業応用まで研究を進めてきました。今後は、ゲノム編集に加えてエピゲノム編集やゲノムイメージングを同時に行うマルチゲノム操作ツールの開発を目指します。さらに、CRISPR技術を基盤として診断から治療までを一体的に実現できる新しいゲノム操作プラットフォームの構築にも挑戦します。これらの研究を通じて、生命現象の理解を深めるとともに、次世代医療につながるゲノム操作技術の創出を目指します。
Representative publications
・Morisaka H et al. CRISPR-Cas3 induces broad and unidirectional genome editing in human cells. Nat Commun. 2019 Dec 6;10(1):5302.
・Yoshimi K, et al. Dynamic mechanisms of CRISPR interference by Escherichia coli CRISPR-Cas3. Nat Commun. 2022 Aug 30;13(1):4917.
・Yoshimi K, et al. Genome editing using type I-E CRISPR-Cas3 in mice and rat zygotes. Cell Rep Methods. 2024 Aug 19;4(8):100833.
3. 宿主-微生物・ウイルス相互作用
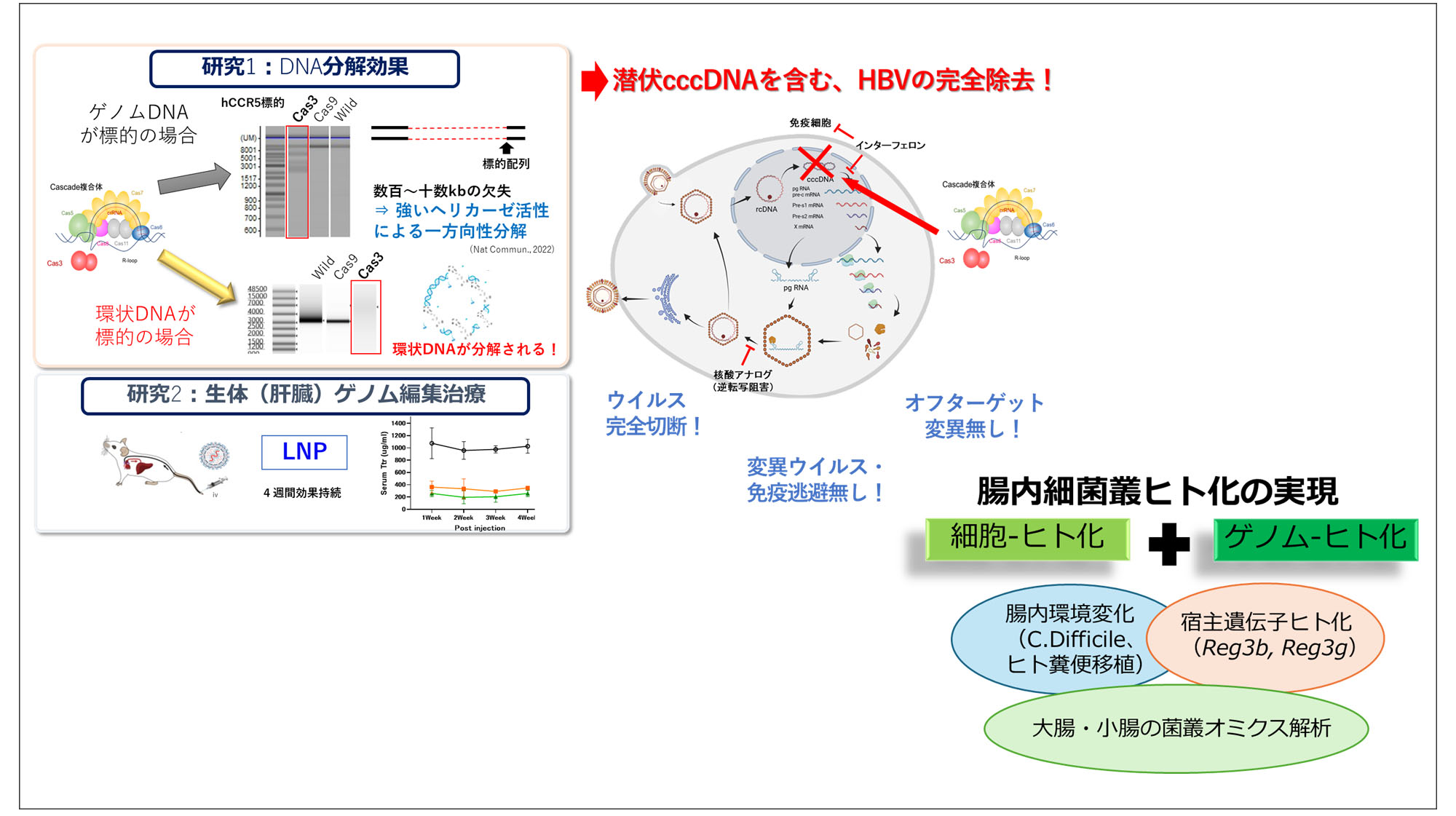
宿主と微生物・ウイルスとの相互作用は、感染症や免疫応答の理解において重要な研究分野です。本研究室では、ゲノム編集技術やヒト化動物モデルを活用し、宿主と微生物・ウイルスの相互作用の分子機構を解析する研究に取り組みます。特に、宿主ゲノム中に潜伏するB型肝炎ウイルス(HBV)などのDNAウイルスの除去戦略の開発に関心を持っています。また、腸管免疫関連遺伝子をヒト化したモデル動物を用いてヒト腸内細菌叢の変化や宿主応答を解析する腸内細菌叢模倣モデルの構築を目指します。さらに、CRISPR技術を利用した感染症の簡易診断法の開発にも取り組み、診断から治療へとつながる新しい感染症研究基盤の構築を目指します。加えて、微生物やウイルスの遺伝子機能の探索を通じて、将来的には新しいゲノム編集ツールの発見につながる可能性も期待しています。
Representative publications
・Hirano R, et al. Next-generation prebiotic promotes selective growth of bifidobacteria, suppressing Clostridioides difficile. Gut Microbes. 2021 Jan-Dec;13(1):1973835.
・Yoshimi K, et al. CRISPR-Cas3-based diagnostics for SARS-CoV-2 and influenza virus. iScience. 2022 Feb 18;25(2):103830.
・Hirano, R, et al. Sustainable and portable CRISPR-based diagnostics for high-sensitivity Mpox detection. npj Biosensing 2, 43 (2025).
4. 実験用ラットの拡充と活用
ラットは生理学、神経科学、薬理学など多くの生命科学研究分野で重要な実験動物です。本研究室では、ゲノム編集技術を活用した遺伝子改変ラットモデルの開発と、研究コミュニティで利用可能なラットバイオリソースの拡充に取り組んでいます。京都大学は世界的なラットリソース拠点である「NBRP-Rat」の中核機関であり、遺伝子改変ラット系統の整備や提供を通して国内外の研究者を支援しています。また、米国のRat Genome Database(RGD)やRat Resource & Research Center(RRRC)、韓国のラットリソース機関などと密接に国際連携を進め、ラットリソースの共有と研究基盤の発展に貢献します。さらに、新しいラット研究データベースの構築やAIを活用した遺伝子機能解析・リソース管理 などにも取り組み、次世代のラット研究基盤の整備を目指します。

